Natriumperiodat, hvitt krystallinsk pulver, løselig i vann, eddiksyre, saltsyre, svovelsyre, salpetersyre, uløselig i etanol. Natriumperjodat er en hvit firkantet krystall som kan løses opp i vann og syre. Den inneholder spor av urenheter som fri syre, klorid, bromid, sulfat og tungmetall. Det kan raffineres ved omkrystallisering fra vandig løsning. Denne typen materiale har sterk oksidasjonsytelse. Selv om det ikke brenner seg selv, kan under visse forhold stoffer som er utsatt for friksjon, vibrasjoner og slag, høy varme eller syre og alkali brytes ned, brenne og eksplodere når de utsettes for fuktighet, organiske stoffer, reduksjonsmidler og stoffer som er uforenlig med naturen. Natriumperjodat har to hovedanvendelser i organisk syntese: som oksidant og katalysator. På grunn av løseligheten utføres oksidasjonsreaksjonen av natriumperjodat vanligvis i vann. Fordi mange organiske kjemikaliebøker er uløselige i vann, er det nødvendig å bruke cosolvent. Når det er en faseoverføringskatalysator eller natriumperjodat er lastet på en inert bærer, kan oksidasjonsreaksjonen også utføres i et tofasesystem.
Natriumperjodat har to hovedanvendelser i organisk syntese: på den ene siden brukes det som oksidasjonsmiddel; På den annen side brukes den som en katalysator. Oksydasjonsreaksjonen til natriumperjodat foregår i vann, men for organisk materiale er det uløselig i vann, så hjelpeløsningsmidlet bør brukes. Når det er en faseoverføringskatalysator sammensatt av kvaternært ammoniumsalt i tofaseløsningen, eller det er en inert bærer på overflaten av oksidasjonsmidlet, kan oksidasjonsreaksjonen også oppstå.
Som en generell oksidant kan natriumperjodat oksidere alkoholer til karbonylforbindelser (formel 1, formel 2)

Natriumperjodat kan også brukes til å bryte glykolforbindelser og oksidere dem til dikarbonylforbindelser (formel 3, formel 4)

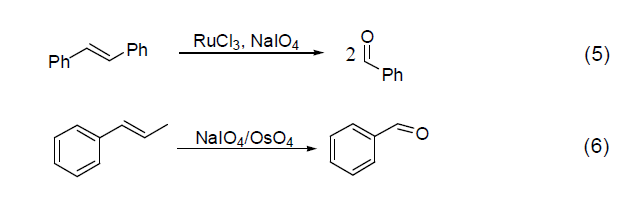
Natriumperjodat bryter til og med C=C-dobbeltbindingen og oksiderer den til karbonylforbindelser. Det kalles det berømte Lemieux-Johnson-reagenset (formel 6) når det kombineres med OsO4 for å oksidere alkener. I tillegg kan reduksjonsproduktene gjenbrukes gjennom periodatoksidasjon.
(Formel 5)
Selektiv oksidasjon av sulfid til sulfoksid er en veldig viktig reaksjon, fordi sulfoksid er et veldig viktig mellomprodukt i organisk syntese. Det kan reagere med natriumperjodat i metanolløsning ved 0 oC. Sulfid vil bli oksidert til sulfon ved høy temperatur eller ved å tilsette for mye natriumperjodat. Når det er sur alumina eller silikagel, kan natriumperjodat selektivt oksidere sulfid til sulfoksid (høyt utbytte kan oppnås ved romtemperatur) (Formel 7, Formel 8). Deltakelsen av faseoverføringskatalysator gjør også at sulfid blir selektivt oksidert til sulfoksid (formel 9)

I tillegg kan natriumperjodat brukes som en billig katalysator for sulfoneringssyntese av arylgrupper (formel 10).

Reaksjonsbetingelsene er meget milde, utbyttet er høyt, reaksjonstiden er kort, og selektiviteten er god.

